近期,由我校李玉龙教授带领的化学合成与应用652科研创新研究团队分别在Organic Letters(IF=5.0,TOP期刊,中国科学院一区期刊,JCR一区期刊)上发表题目为“Ni-Catalyzed Asymmetric Reductive Arylation and Alkenylation of N‑Sulfonyl Imines”和Science China Chemistry(IF=9.7,TOP期刊,中国科学院一区期刊,JCR一区期刊)上发表题目为“Enantioselective α-Aryl/Alkenylation of N-Sulfonyl Amines via Relay Heterogeneous and Homogeneous Pd/Rh Catalysis”的学术论文。四川轻化工大学为论文第一单位和通讯单位,化学与环境工程学院青年教师刘玉成博士为论文第一作者和共同通讯作者,李玉龙教授为论文共同通讯作者。
手性α-支链胺广泛存在于天然产物、药物分子和手性配体中,开发高效构建该类骨架的方法是有机合成化学的研究前沿之一。过渡金属催化的不对称官能化反应已成为合成手性胺的重要方法,为从简单原料快速构建复杂分子提供了有效工具。两篇论文的具体研究工作如下:
1. Ni-Catalyzed Asymmetric Reductive Arylation and Alkenylation of N‑Sulfonyl Imines
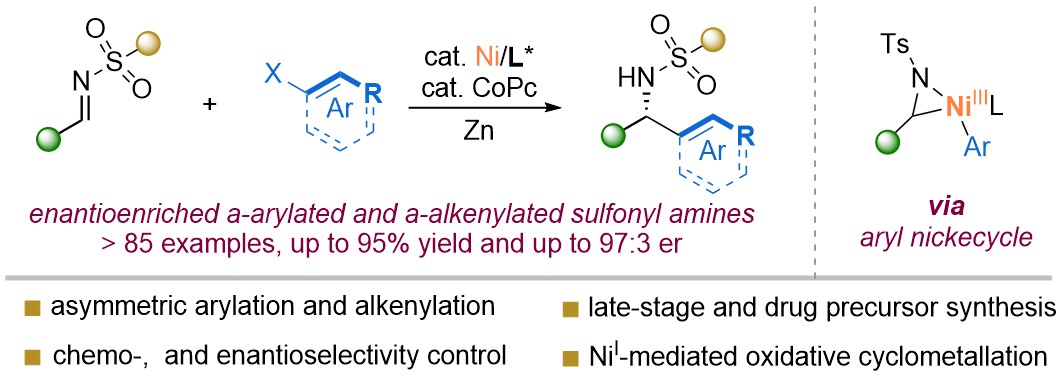
该论文报道了一种镍催化的不对称还原偶联新策略,成功实现了N-磺酰亚胺与芳基/烯基碘化物的高对映选择性反应。研究通过改性的手性联咪唑配体与钴酞菁(CoPc)协同催化,在温和条件下(10°C)即可获得高达94%的收率和95.5:2 er的对映选择性。该方案展现出优异的底物普适性(>85底物),兼容卤素、酯基、杂环等敏感官能团,并成功实现了萘普生、布洛芬等复杂药物分子的后期修饰。DFT计算支持反应通过Ni(I)介导的氧化环金属化路径进行,形成关键的氮杂镍环中间体。本研究发展了一种条件温和、适用范围广的手性胺合成方法,为廉价金属催化不对称合成及药物分子修饰提供了重要参考,具有显著科学意义与应用前景。
论文链接:https://doi.org/10.1021/acs.orglett.5c04872
2. Enantioselective α-Aryl/Alkenylation of N-Sulfonyl Amines via Relay Heterogeneous and Homogeneous Pd/Rh Catalysis
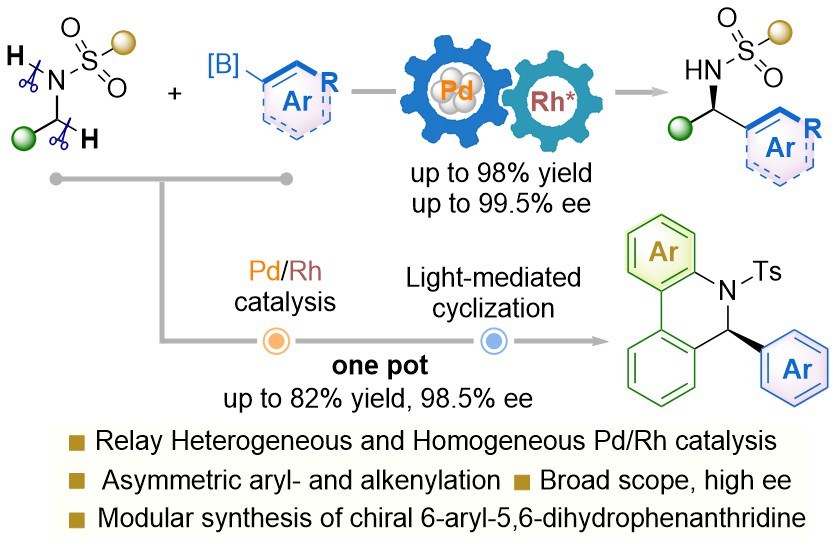
该论文发展了一种新颖的非均相相钯与均相铑接力催化体系,首次实现了N-磺酰基胺的直接不对称α-C–H键芳基化与烯基化反应。该策略的核心在于:非均相钯催化剂(如Pd(OAc)₂)在溴苯作为温和氢受体的作用下,实现N-磺酰基胺的去饱和化反应,原位生成N-磺酰亚胺中间体;随后,手性铑催化剂(如[Rh(L2)Cl]₂)对该中间体进行高对映选择性的芳基或烯基加成,最终获得手性α-支链胺。该方法克服了传统方法对环状胺的限制,成功应用于多种直链、苄位及位阻较大的胺类底物,产物收率高达98%,对映选择性最高可达99.5% ee。此外,该策略还被扩展至手性6-芳基-5,6-二氢菲啶类化合物的合成。机理研究表明,钯催化的去饱和化步骤为非均相催化过程,而均相铑催化的加成步骤速率远快于背景反应,是高对映选择性的关键。该研究为惰性C–H键的直接不对称官能化提供了新思路。
论文链接:https://www.sciengine.com/SCC/doi/10.1007/s11426-025-3314-2
上述研究工作得到国家自然科学基金项目、四川轻化工大学人才引进项目和652科研创新研究团队项目的经费资助。
【复审:张国成 终审:许筠柱】






